1.细胞病理论
- 人只有一种病:细胞病
细胞是人体基本的组成单元,人体大约由200多种、36万亿个细胞组成。疾病、衰老都源于细胞炎症,细胞炎症 → 组织炎症→器官功能衰退→系统功能紊乱→ 引发人体疾病/衰老。
- 细胞为什么会得病?
炎症的诱因:组织损伤或异物侵入、饮食中的促炎食品、慢性炎症持续存在。
炎症影响机制:引发氧化应激→ 影响基因表达→ 细胞受损→ 细胞功能衰退→导致疾病/加速全身衰老进程。
iPSC外泌体通过携带生物活性分子,能够精准调控细胞功能,修复损伤组织,实现疾病的根本性治疗。
2.iPSC&Exosome简介
- iPS细胞
定义:是将成熟体细胞(如皮肤成纤维细胞、血细胞)经人工重编程,逆分化为具有类似胚胎干细胞(ESC)特性的多能干细胞,可无限增殖并分化为三胚层各类细胞。
经典诱导:通过导入Oct4、Sox2、Klf4、c‑Myc四种转录因子(山中因子)实现重编程;现已有质粒、腺病毒、小分子药物等非整合诱导方案,提升安全性。
核心特征:
全能分化:可分化为内、中、外三胚层来源的各类细胞(如心肌、神经、胰岛细胞)。
无限增殖:体外可大量扩增,满足研究与临床的规模化需求。
低伦理风险:源于成体细胞,规避胚胎干细胞相关伦理争议。
低免疫排斥:可取自患者自体细胞,降低移植排斥风险
- iPSC外泌体
定义:是由诱导多能干细胞分泌的直径为30-150nm 的纳米级囊泡,携带有母细胞的蛋白质、miRNA、mRNA、脂质等生物活性成分。它结合了iPSC的再生潜能与外囊泡的高效递送特性,成为疾病治疗及抗衰老领域的新型再生医学工具。
核心特性:
多能性继承:iPSC外泌体保留了iPSC的全能性信号分子(如Oct4、Sox2、Nanog等相关miRNA),可调控靶细胞的基因表达,促进组织修复与再生。
低免疫原性:iPSC外泌体不含细胞核,避免了iPSCs直接移植可能引发的免疫排斥或致瘤风险。
靶向递送能力:通过膜表面蛋白与受体细胞特异性结合,精准递送功能分子至损伤或衰老组织
3.iPSC&Exosome产业路径图
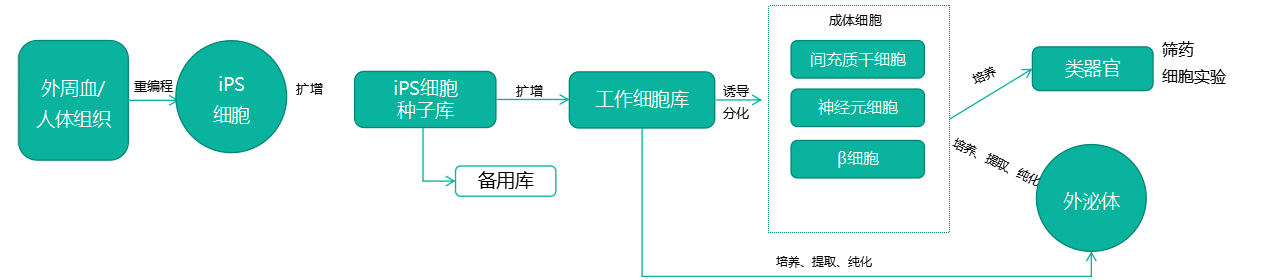
4.iPSC外泌体的特点

5.与其他干细胞及外泌体的对比
- iPSC外泌体 vs 间充质干细胞
.jpg)
- iPSC外泌体 vs 间充质干细胞外泌体
.jpg)
产品管线
产品管线一:IIT临床研究及临床应用转化
佩格赛斯目前的候选产品管线包括iPSC外泌体和工程化的外泌体,现已开展的主要适应症研究涵盖了烧伤、医美术后修复、膝关节疼痛、缺血性脑卒中、2型糖尿病、慢阻肺/肺纤维化、高血压、肥胖减重等多种疾病。
1. 烧伤、医美术后修复
烧伤或医美术后,皮肤屏障功能严重受损,防御能力下降,水分流失增加,感染风险急剧上升。成纤维细胞功能异常,增殖速度减缓,胶原合成能力下降。胶原合成呈现紊乱状态,I型和III型胶原比例失衡,导致瘢痕过度增生或愈合延迟。
作用机制:
- 促进成纤维细胞增殖:iPSC外泌体上调N-cadherin、cyclin-1、PCNA等关键基因表达,显著提升成纤维细胞的增殖活性和胶原合成能力
- 加速上皮再生:携带的miRNA和生长因子激活皮肤干细胞,促进角质形成细胞迁移,加速创面再上皮化进程,快速闭合伤口
- 调节胶原合成:早期促进I型和III型胶原合成,后期抑制过度胶原沉积,实现平衡修复,减少瘢痕形成
- 促进血管新生:刺激血管内皮细胞增殖和迁移,改善创面血供,为修复提供充足营养
2. 膝关节疼痛
骨关节炎(OA)是全球中老年人致残的第二大原因。病理核心为软骨进行性退变,伴随滑膜炎症、神经敏化、力学失衡等。炎症因子IL-6和MMP13高表达,降解软骨基质,II型胶原合成减少,导致关节疼痛、僵硬和功能障碍。传统治疗仅缓解症状,无法修复受损组织。
作用机制:
- 降低炎症因子表达:外泌体携带的miRNA通过抑制NF-κB信号通路,显著降低IL-6、MMP13等促炎因子表达,减轻关节炎症
- 软骨基质修复:激活软骨细胞合成II型胶原(COL2A1),修复受损软骨基质,恢复软骨结构和功能
- 保护软骨细胞:抑制软骨细胞凋亡,促进细胞增殖和迁移,维持软骨细胞数量和健康状态
- 局部精准作用:关节腔注射后,外泌体在72小时内局限于给药部位,未显著迁移至其他器官,安全性良好
3. 缺血性脑中风
缺血性中风约占脑中风发病的70%–80%,会造成脑局部组织损伤和全身多系统继发性损伤两大层面:通过缺血级联反应对神经元细胞造成损伤,星形胶质细胞形成瘢痕、少突胶质细胞髓鞘受损、小胶质细胞引发炎症——共同构成了阻碍修复的微环境,还会通过全身炎症风暴、神经 – 体液调节紊乱、灌注异常等机制引发多外周器官的继发性损伤。
作用机制:
- 神经元保护:通过miRNA(如miRNA-22-3p、miRNA-760)抑制凋亡、焦亡及铁死亡,保护半暗带神经元。
- 神经元再生与修复:富含BDNF(脑源性神经营养因子) 和 GDNF(胶质细胞源性神经营养因子),被直接递送至受损的脑区(如黑质),促进内源性神经干细胞分化为多巴胺能神经元,促进突触形成。
- 抗炎调控:通过抑制炎症因子如IL-6和TNF-α的产生,减轻炎症反应,同时激活抗炎细胞因子IL-10,抑制小胶质细胞过度活化。
- 联合作用机制:鼻喷给药(神经细胞外泌体)重点治疗脑内局部损伤,静脉注射(iPSC 外泌体)全面治疗全身炎症及保护外周器官的协同体系,共同阻断缺血级联损伤、促进神经功能恢复,通过差异化细胞修饰,实现中枢 – 外周炎症同步干预、结构 – 功能双重修复,加速神经功能恢复进程。
4. 心梗后心肌修复
心肌梗死(MI)导致心肌细胞大面积坏死,心脏收缩功能急剧下降,左室射血分数(LVEF)降低。梗死区域发生病理性心室重构,心肌被纤维瘢痕组织替代,进一步损害心脏功能,最终可能导致心力衰竭。
作用机制:
- 抗凋亡保护:携带抗凋亡因子(TNF-α等),抑制Caspase促凋亡通路、解除SOCS2/PATEN的抑制作用、保护线粒体功能,最终减少心肌细胞凋亡,改善心脏功能并逆转不良心肌重塑。
- 促血管生成:释放VEGF、胎盘生长因子等,促进新生血管形成,改善梗死区域血供
- 抑制纤维化:抑制心肌成纤维细胞的活化和胶原沉积,抑制 TGF-β通路,减少细胞外基质过渡沉积,防止心室重构,改善心肌顺应性和收缩功能
5. 2型糖尿病
2型糖尿病核心病理为胰岛β细胞数量减少或功能受损,导致胰岛素分泌不足。同时外周组织(脂肪、肌肉)出现胰岛素抵抗,葡萄糖摄取和利用能力下降,血糖升高。预计到2045年中国糖尿病患者将增至1.5亿,亟需突破性治疗方案。传统治疗无法从根本上修复胰岛功能。
作用机制:
- 促进β细胞增殖:外泌体携带的miRNA激活β细胞增殖相关基因,促进受损胰岛组织修复与再生
- 抑制β细胞凋亡:抑制胰岛β细胞凋亡信号通路,减少β细胞死亡,保护残存胰岛功能
- 改善胰岛素敏感性:调节脂肪细胞、肌肉细胞胰岛素信号通路,增强葡萄糖摄取和利用能力
- 联合治疗:采用iPSC诱导胰岛 β 细胞外泌体联合iPSC外泌体注射给药,治疗2 型糖尿病,针对 2 型糖尿病胰岛 β 细胞功能衰退、胰岛素分泌不足、抗凋亡能力弱的核心问题,细胞修饰的核心目标是保护胰岛 β 细胞存活、增强胰岛素合成与分泌功能、提升其抵抗高糖 / 炎症损伤的能力;强化外泌体的胰岛素增敏活性、提升靶组织靶向性,通过对 iPSC 供体细胞及外泌体的双重改造,使其精准作用于肝脏、肾脏、骨骼肌、脂肪等胰岛素抵抗靶器官,高效调控胰岛素信号通路并抑制炎症、抑制肝糖异生。
6. 慢阻肺/肺纤维化
慢性阻塞性肺疾病(COPD)和肺纤维化是以肺组织进行性损伤为特征的严重慢性肺部疾病。病理核心为长期炎症刺激导致肺泡上皮细胞损伤,肺泡结构破坏,气体交换功能下降。上皮-间质转化(EMT)导致肺泡上皮细胞异常转变为成纤维细胞,肺部胶原过度沉积,肺纤维化进行性加重。传统治疗仅能延缓进程,预后差。
作用机制:
- 精准靶向直达病灶:雾化技术将外泌体制成1-5微米气溶胶颗粒,随呼吸直接抵达肺泡,避免全身循环损耗;
- 强力抗炎调节免疫:通过静脉注射,作用于全身免疫系统,抑制巨噬细胞过度释放TNF-α、IL-6等促炎因子,增加抗炎因子IL-10,重塑肺部免疫平衡;
- 抑制肺纤维化:通过抑制Wnt/β-catenin信号通路,阻断上皮-间质转化,减少胶原沉积,延缓甚至部分逆转肺纤维化;
- 修复受损肺泡:促进肺泡上皮细胞增殖和分化,修复受损肺泡结构,改善气体交换功能。
7. 高血压
高血压的发病机制复杂,涉及多种因素的相互作用。主要包括交感神经系统紊乱、肾素 – 血管紧张素 – 醛固酮系统(RAAS)亢进、肾脏水钠代谢异常以及血管结构和功能异常。这些机制并非孤立存在,而是相互影响,共同导致外周血管阻力增加和血压升高。
作用机制:
- 修复血管内皮功能:MSC / 内皮细胞外泌体携带 miR-126、VEGF、ACE2,促进 NO 合成、抑制内皮素 – 1,改善血管舒张;降低氧化应激,减少内皮损伤。
- 逆转血管重构:递送 miR-21/miR-155、TGF-β 等,抑制平滑肌细胞增殖与胶原沉积,减轻血管壁增厚 / 管腔狭窄,降低外周阻力;拮抗 miR-320d/423-5p 可缓解自发性高血压大鼠动脉重塑。
- 调控 RAAS 平衡:外泌体携带 ACE2、miR-155 等,抑制 AngⅡ 生成、促进其降解,减少醛固酮分泌与水钠潴留,降低血压波动。
- 靶器官保护:抑制心肌病理性肥大、延缓心肌重构;保护肾小球内皮,减少蛋白尿、延缓肾小球硬化。
- 调节神经体液:抑制交感过度激活,减少肾钠重吸收,降低心输出量与外周阻力。
8. 肥胖减重
肥胖的病理本质是机体长期处于能量正平衡(能量摄入>能量消耗),并伴随中枢能量平衡调控紊乱、外周脂肪组织代谢失衡、内分泌网络失调的多维度病理改变,最终导致白色脂肪组织(WAT)过度增殖与肥大,棕色脂肪组织(BAT)产热耗能功能缺陷,同时继发胰岛素抵抗、瘦素抵抗等代谢紊乱,形成 “脂肪堆积 – 代谢紊乱 – 脂肪进一步堆积” 的恶性循环。
作用机制:
- 靶向调控腹部脂肪代谢,减少腹脂堆积:腹部局部注射实现外泌体在腹部皮下 / 内脏脂肪的高浓度富集,
诱导腹部 WAT 褐变,转化为功能性米色脂肪;
精准调控局部脂肪褐变、分解,减少腹脂堆积;
改善内脏脂肪的慢性炎症微环境,恢复腹部脂肪组织的正常代谢功能
- 全身调控能量代谢,提升基础耗能 :外泌体经血液循环穿透血管内皮屏障,到达全身内源性 BAT、下丘脑、肝脏、骨骼肌、肠道等代谢关键器官,
激活全身 BAT 产热,上调 UCP1 表达,显著提升机体基础能量消耗(REE)
修复中枢能量调控,让瘦素、胰岛素重新发挥 “抑摄食、促耗能” 的作用,减少高热量饮食摄入;
改善肝脏 / 骨骼肌胰岛素抵抗、调节肠道菌群,实现全身基础能量消耗提升和摄食抑制,避免脂肪全身再堆积
产品管线二:iPS细胞及成体细胞库
1. iPSC主细胞库(MCB)与工作细胞库(WCB)
2. 分化的成体细胞库:免疫细胞、间充质基质细胞、β细胞、神经元细胞、滑膜细胞、心肌细胞等
产品管线三:免疫细胞治疗实体瘤
iPSC诱导分化的四大免疫细胞产品,iPSC-NK细胞、iPSC-巨噬细胞、iPSC-DC细胞、iPSC-CIK细胞,用于实体瘤(肺癌、肝癌、乳腺癌等)
